|
|
| Le financement de ce site est assuré par vos dons, merci! | |
|
|
|
|
|||||
|
|
|||||||
|
|
|
|
|
|
|
|
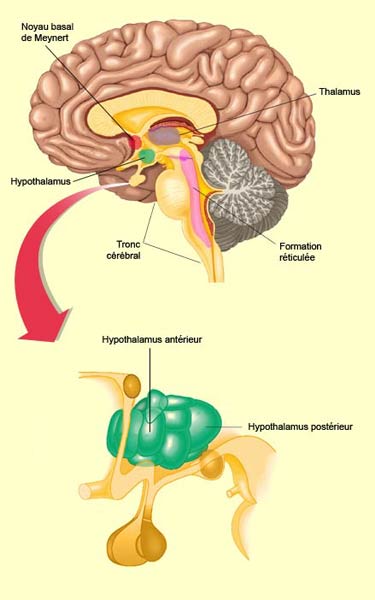
La régulation de l’éveil, vitale pour la survie, mets en jeu plusieurs structures redondantes. Aucune des structures décrites, prise isolément, n’est indispensable à l’activation corticale. Mais trois structures cérébrales qui envoient des projections au cortex sont suffisantes au maintien de la désynchronisation de l’EEG propre à l’éveil. On les désigne souvent comme le « réseau exécutif de l'éveil ». Il s’agit de l’hypothalamus postérieur, du télencéphale basal et de la partie intra-laminaires du thalamus. La stimulation de l’hypothalamus postérieur produit un état d’éveil comparable à celui que l’on obtient par la stimulation de la formation réticulée du tronc cérébral. L’activité de l’hypothalamus postérieur diminue d’ailleurs naturellement au cours du sommeil, relâchant alors moins d’histamine, une molécule utilisée comme neurotransmetteur par l’hypothalamus postérieur. Les antihistaminiques que l’on prend contre les manifestations allergiques provoquent d’ailleurs une certaine somnolence en diminuant l’activité de l’histamine.
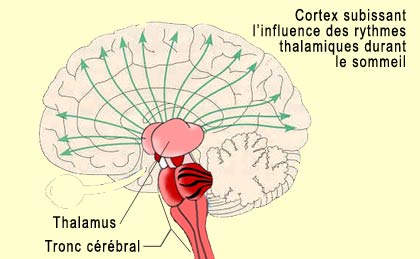
Dans les cas qui précèdent, l’activation du cortex responsable de l’éveil résulte de la stimulation directe des neurones corticaux par les différents éléments du réseau de l’éveil. Mais ces neurones corticaux peuvent être activés d’une autre manière : par l’inhibition des neurones qui inhibent naturellement l’activité corticale. C’est exactement ce que font des neurones GABAergiques localisés dans l’hypothalamus postérieur et dans le télencéphale basal : ils inhibent d’autres neurones GABAergiques corticaux. Ce réseau exécutif de l’éveil est lui-même activé par d'autres systèmes venant du tronc cérébral. C’est donc l’ensemble de ces signaux d’éveil qui vont cesser de parvenir au cortex avec l’avènement du sommeil lent. Ils seront interrompus au niveau du thalamus, véritable carte d’accès au cortex qui est grandement influencée par les systèmes neuromodulateurs diffus du tronc cérébral.
Plus précisément, c’est l’activité rythmique qui se met alors en place dans les neurones thalamo-corticaux de la région intra-laminaire du thalamus qui provoque cette déconnexion corticale des signaux internes et externes. En revanche, durant les phases paradoxales du sommeil, le transfert des signaux à travers le thalamus est probablement en partie respecté, du moins sous un aspect fragmentaire, filtré ou déformé. Finalement, on ne saurait passer sous silence le rôle fondamental que joue l’hypothalamus antérieur dans l’endormissement. Celui-ci, et notamment sa région préoptique, serait sensible à l'influence de la sérotonine libérée au cours de l'éveil. Le sommeil serait alors favorisé par l’activation de cette région préoptique de l’hypothalamus antérieur qui va pouvoir inhiber l'hypothalamus postérieur par l’entremise de ses neurones GABAergiques. Des lésions de ces neurones GABAergiques provoquent d’ailleurs des insomnies, et leur stimulation provoque un endormissement rapide.
|
|
||||||||||||||||||||||||||||||||||||||||
|
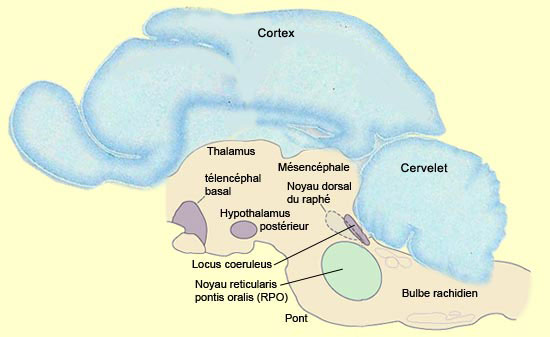
Si l’amygdale est l’une des régions cérébrales les plus actives durant le sommeil paradoxal, c’est plutôt dans les profondeurs du tronc cérébral qu’est généré cet état du cerveau. Ceci dit, il ne faut pas voir l’ensemble des structures corticales et limbiques impliquées dans le sommeil paradoxal comme subissant passivement des ordres venus du tronc cérébral. Au contraire, l’imagerie onirique particulière associée au sommeil paradoxal est le fruit d’une interaction dynamique entre certaines structures clés du tronc cérébral et le reste de l’encéphale. C’est la découverte que le sommeil paradoxal était présent chez presque tous les mammifères qui ouvrit la porte aux premières expérimentations animales par Michel Jouvet au début des années 1960. Des études de lésions et de stimulations électriques en particulier chez le chat permirent de circonscrire progressivement au tronc cérébral les neurones à l’origine du sommeil paradoxal. L’une de ces approches consiste à diviser le cerveau en deux parties et d’essayer de voir laquelle des deux conserve l’activité de la fonction recherchée. On répète ensuite l’opération dans la moitié « gagnante » pour circonscrire encore d’avantage la région impliquée, et ainsi de suite jusqu’à ce qu’on isole certains noyaux essentiels. Comme chaque partie du cerveau est souvent densément interconnectée avec les autres, on aurait pu penser que la moindre subdivision du cerveau aurait détruit l’activité électrique propre au rêve. Mais étonnamment, les régions du tronc cérébral génératrices du sommeil paradoxal peuvent garder leur activité fonctionnelle même si elles sont déconnectées de pratiquement tout le reste de l’encéphale. À l’inverse, la destruction d’une toute petite portion du tronc cérébral peut prévenir l’expression du sommeil paradoxal. Quels sont donc ces noyaux, localisés dans une très petite portion du tronc cérébral, qui sont à la fois nécessaires et suffisants à l’activité nerveuse du sommeil paradoxal ? Essentiellement, ils sont dans la protubérance (aussi appelée le pont), et particulièrement dans sa partie rostrale qui fait jonction avec le mésencéphale. Un noyau fondamental pour le sommeil paradoxal est le noyau reticularis pontis oralis (RPO) qui s’étend du mésencéphale caudal à la protubérance rostrale. Une population de neurones dans cette région est sélectivement active durant le sommeil paradoxal. Les études de lésion de cette petite région du tegmentum pontique ont également montré qu’elle était requise pour avoir un sommeil paradoxal normal.
Le sommeil paradoxal peut être provoqué par microinjection d’agonistes de l’acétylcholine dans cette petite région dont on ignore si elle est suffisante pour la génération de tous les aspects du sommeil paradoxal comme l’est par exemple le noyau suprachiasmatique pour notre cycle circadien. Cette élévation soudaine de l’activité des neurones cholinergiques de la protubérance (ou pont) nécessaire à l’apparition du sommeil paradoxal peut sembler pour le moins étrange étant donné que les systèmes à acétylcholine sont reconnus pour leur rôle dans l’éveil. Comment expliquer qu’un système associé à l’éveil comme le l’acétylcholine soit activé pendant l’une de nos phases de sommeil ? La réponse réside probablement dans la diminution parallèle de l’activité de deux autres noyaux produisant d’autres neurotransmetteurs de l'éveil, diminution tout aussi nécessaire à l’avènement du sommeil paradoxal : le noyau dorsal du raphé, un amas de neurones sérotoninergiques, et le locus coeruleus, un groupe de neurones noradrénergiques, tous deux situés dans la partie rostrale de la protubérance. Le sommeil paradoxal ne peut apparaître que si toute activité a
cessé dans ces deux systèmes aminergiques principaux
du tronc cérébral. On peut parler en quelque sorte
d’un système permissif pour ces neurones à sérotonine
et à noradrénaline (qu’on qualifie aussi
de SP-Off pour
désigner leur inactivité durant le sommeil paradoxal)
dans le sens où le sommeil paradoxal ne devient possible
que lorsque leur activité a cessé. L’arrêt
de cette activité pourrait par exemple aider à la
suppression de la
conscience durant le sommeil paradoxal. Les périodes
de sommeil paradoxal se terminent d’ailleurs quand les
neurones aminergiques redeviennent actifs. |
| |
|
|
|
|
|
|
|
|